消化管外科
消化管外科 患者の皆さまへ
消化管外科のご紹介

消化管外科では、胃や大腸の悪性腫瘍を中心に診療を行なっています。また、胃・十二指腸潰瘍穿孔、大腸穿孔、急性虫垂炎などの急性腹症に対する救急医療も実践しています。
消化管悪性腫瘍の診療に際しては、個々の進行度や病態に応じた最適な治療を提供することを心がけています。診断においては通常の内視鏡検査やレントゲン検査の他、超音波内視鏡検査や拡大内視鏡検査などを用いて、病変の広がりと深さを正確に診断することを心がけています。
早期がんや中期がんの治療においては、治療後の患者さんの術後Quality of life (QOL) の向上を目的にした低侵襲治療や機能温存治療を優先して選択し、チーム医療を実践しています。
低侵襲治療として、早期悪性腫瘍に対する内視鏡治療や早期および中期悪性腫瘍に対する腹腔鏡下手術やロボット手術を実践しており、我が国において指導的立場にあります。
一方、機能温存治療として、胃切除では噴門側胃切除細径胃管再建術などを、直腸切除においては自律神経温存手術を施行しています。
進行がんの治療においては、抗がん剤治療、放射線治療などを手術治療に併用して実施しています。
以上のように、消化管悪性腫瘍の診療においても、患者さん本位の医療を実践するために、診断は科学的に、そして治療に際しては進行度に応じた個別治療を行い、心温まるケアとともに質の高いチーム医療を提供しております。
消化管外科への質問
- 腹腔鏡による胃の手術とはどのようなものですか?
-
腹腔鏡下胃切除術といいます。従来から行われてきた開腹手術(お腹を開けて行う手術)に比べて、患者さんのからだにかかる負担が少ないとされています。
- 【患者さんにとっての腹腔鏡下胃切除術のメリット】
-
- 手術による傷が開腹手術に比べて小さく、手術後の痛みが軽くなります。
- 術後のからだの回復が早く、退院や日常生活への早期復帰が可能です。
- 手術中の出血量が少ないです。
- 手術後の合併症の発生(肺炎や腸閉塞症〈腸がつまること〉など)が少なくなります。
≪対象となる患者さん≫
腹腔鏡下胃切除術の対象となる患者さんは、早期胃がんの方です。2021年に発行された「胃がん治療ガイドライン(第6版)」においても、『幽門側胃切除術が適応となるステージI期(早期胃がん)の症例で、腹腔鏡下手術は日常診療の選択肢となりうる』と位置づけられています。
しかし近年では、当科のように日本の中でも指導的立場で腹腔鏡手術を行ってきた施設においては、進行胃がんに対しても可能な限り積極的に腹腔鏡下手術を行っています。 - 胃を切除したあとの食べ物の通り道はどうなるのですか?
-
胃を切除したあと、食べ物の通り道を作ることを「再建」といいます。
胃切除術後の再建術式には、いくつかの方法がありますが、当科ではRoux-en-Y法(ルーワイ法)で行うことがほとんどです。
他の方法と比較したルーワイ法の長所と短所を図に示します。-
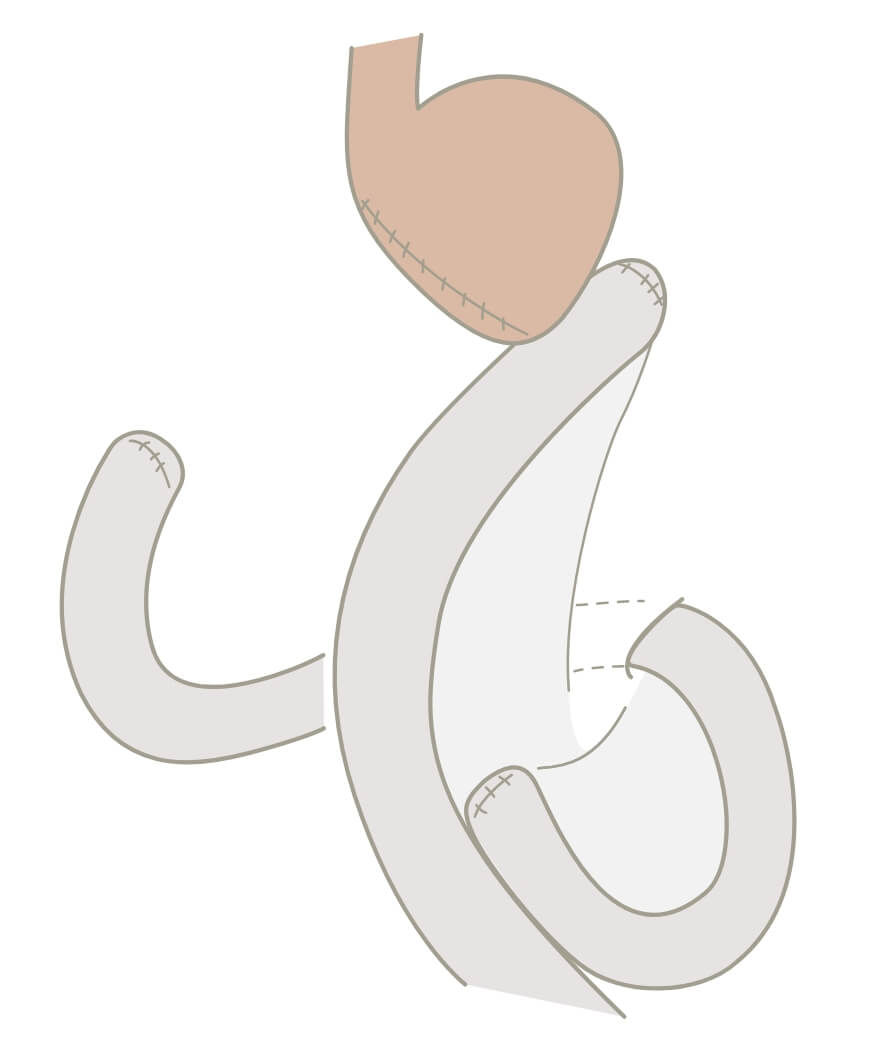 ▲幽門側胃切除術後のルーワイ再建法
▲幽門側胃切除術後のルーワイ再建法
-
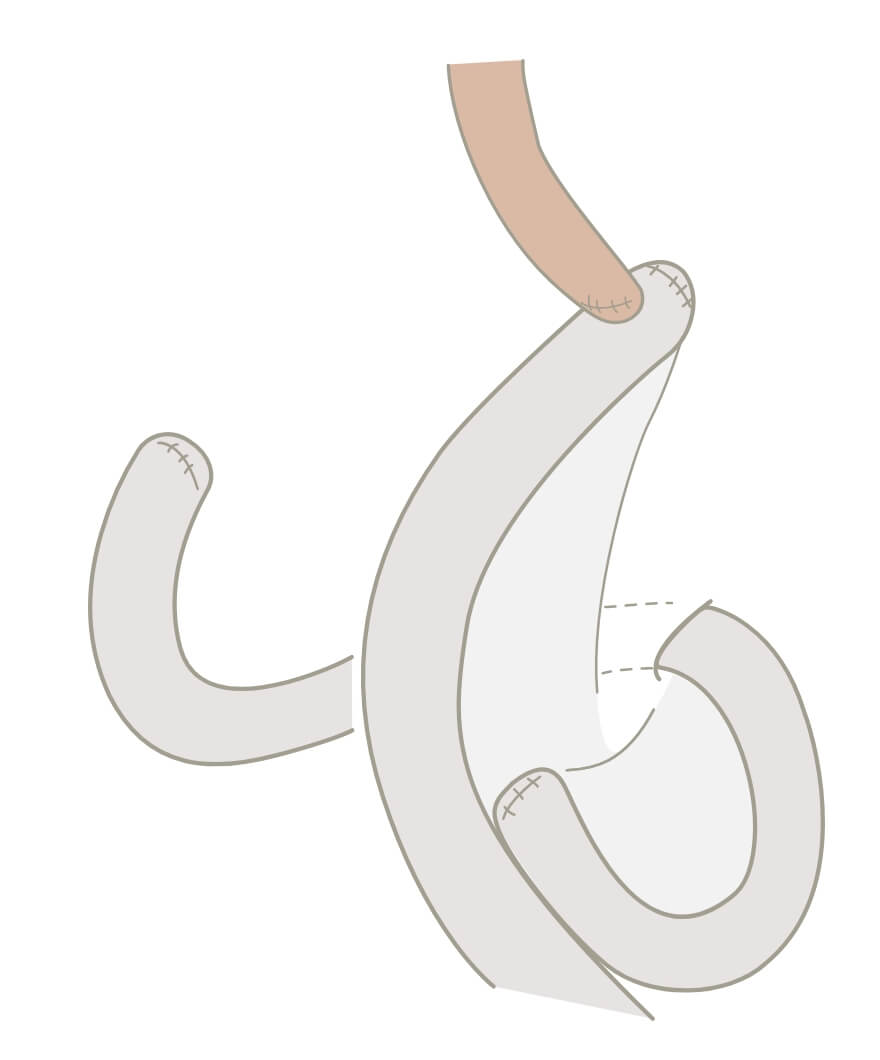 ▲胃全摘術後のルーワイ再建法
▲胃全摘術後のルーワイ再建法
-
- 直腸がんに対する機能温存手術について教えてください。
-
直腸の周囲には、排尿や性機能をつかさどる自律神経がとおっています。直腸がんの手術では、微小ながんを取り残さないようにこれら自律神経近くの組織まで摘出する必要があるため、術後の性機能障害や排尿障害が問題になることがあります。
また、直腸がんの手術では、がんの位置が肛門に近いため、人工肛門造設が必要となることもあります。
しかし近年では、腹腔鏡手術やロボット手術により、肛門に近い位置のがんの手術の際にも細かい解剖が認識できるので、自律神経の温存や肛門括約筋の温存が可能となりました。泌尿生殖機能を維持しつつ、腸管吻合法・永久人工肛門を回避し、肛門機能が温存できる機会が増えています。当科では、それらの手術を標準的に行っており、より肛門に近い直腸癌に対する究極の肛門温存手術である括約筋間直腸切除術(ISR)による肛門機能の温存を積極的に施行しています。 - 局所進行直腸癌の集学的治療法について教えてください。
-
肛門に近い直腸がんは、大腸がんの中でも手術後の再発率が高いことが知られています。特に高度に進行した直腸がんでは、せっかくがんを切除しても、その近くに再発することがあります。これらの進行したがんに対する治療には、外科的切除だけでは限界があり、他の治療を組み合わせる必要があります。
当科では、肛門に近い高度に進行した直腸がんに対しては、手術前に放射線治療と抗がん剤治療を行って、がんの縮小を図り手術をする集学的治療を行うことがあります。手術前にこれらの治療を行うことで手術後の再発率を低下させます。また、従来の手術だけの治療法では人工肛門が不可避であった場合でも、がんの縮小によって、人工肛門を回避し肛門温存できることがあります。
- 食道がんに対する低侵襲手術について教えてください。
-
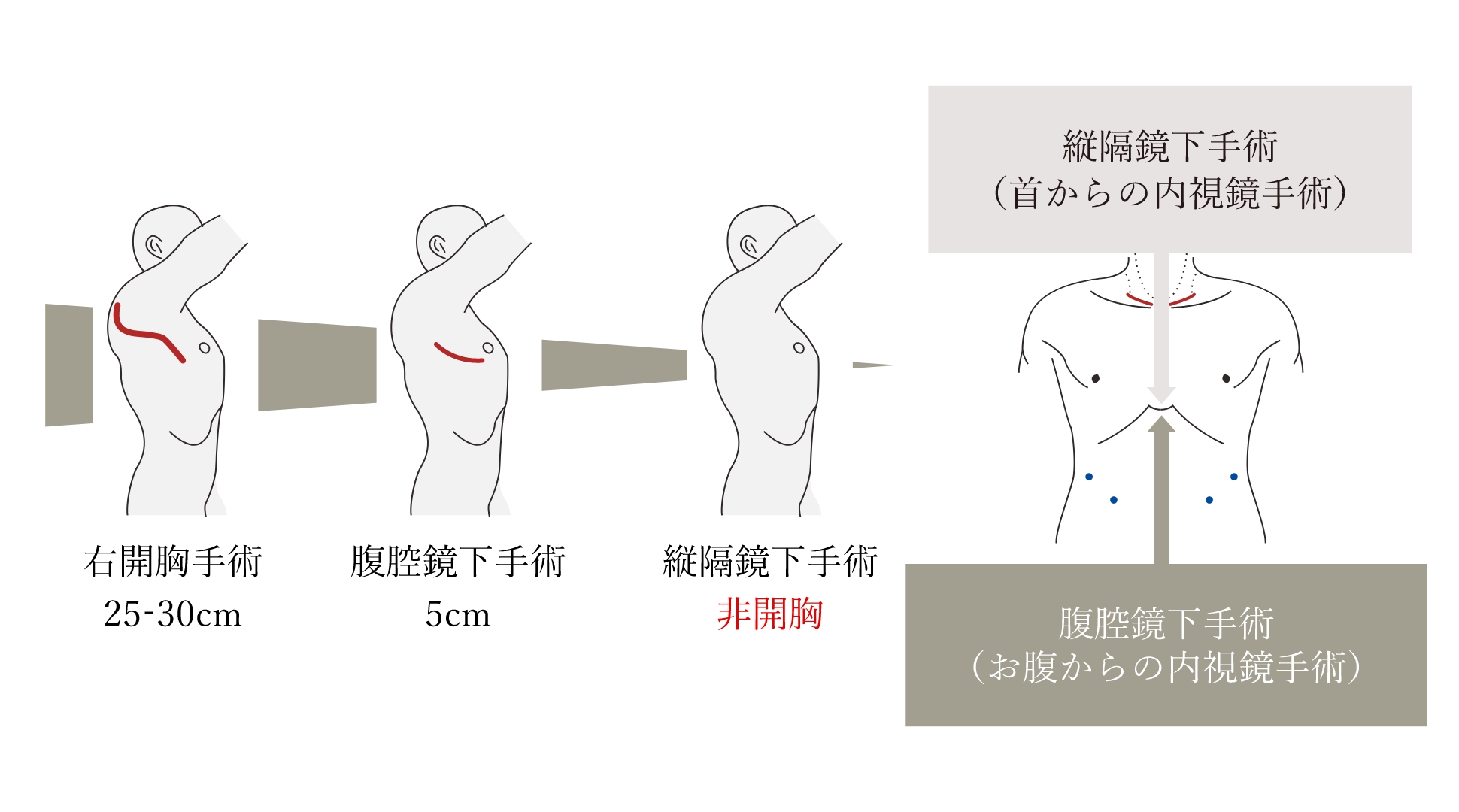
食道は首からお腹につながる臓器であり、従来の食道がん手術では首と胸とお腹の3箇所から手術をする必要があります。食道がんの手術では術後呼吸器合併症(肺炎など)が重要な問題であり、胸部の手術操作(傷の大きさなど)を最小限にする工夫がされています。縦隔鏡(じゅうかくきょう)手術は胸の傷(開胸操作)を必要とせず、術後の呼吸機能保持に有用とされています。我々は2017年から縦隔鏡手術を導入し、これまで安全に施行してきました。

- 食道がんの再発に対する治療法について教えてください。
-
食道がんに対しては手術療法の他に、抗がん剤と放射線の併用療法が行われることもあります。放射線療法後の再発や遺残(がんが残る)に対する追加治療は体への負担が大きく、また手術も複雑となるため、追加治療法の選択は慎重に行う必要があります。放射線療法後の新しい低侵襲治療として光線力学療法が2015年に保険収載され、当科では2018年に導入し、その有用性を報告しました。
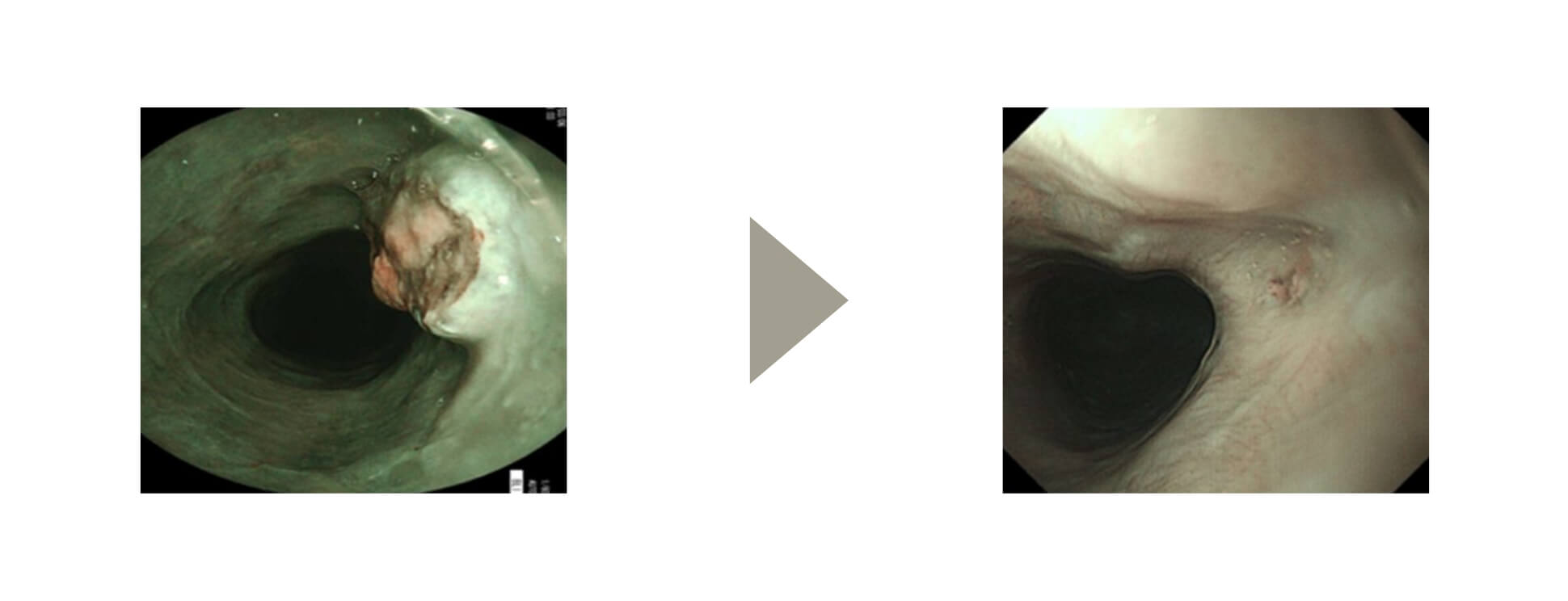 光線力学療法によるがん消失
光線力学療法によるがん消失
消化管外科 臨床診療
消化器グループにおける臨床の3本柱
新しい低侵襲手術手技の開発・導入と定型化
- 食道癌に対する縦隔鏡下非開胸食道手術の導入
- 胃癌に対する腹腔鏡手術の適応拡大、上部胃癌手術の定型化
- 大腸癌に対するTaTME,腹腔鏡下側方郭清、ロボット支援手術
食道癌手術では縦隔鏡下食道手術を開始し良好な成績を示しています。
当科で1993年に胃癌に対する腹腔鏡下胃切除術は発展期を迎え、進行胃癌への適応拡大と安全性の確立に努めています。大腸癌に対する腹腔鏡下手術もTaTME,ロボット支援手術を導入し低侵襲手術を追求しています。
集学的治療の開発
- 周術期化学療法(胃・食道)および化学放射線治療(直腸)
- 周術期リハビリテーション、多職種チーム連携
予後向上の取り組みとして、抗がん剤あるいは放射線治療と、低侵襲手術を組み合わせた集学的治療を推進しています。
臨床研究プロジェクト
- 大分からのエビデンス発信(Oita trial,講座内での臨床研究)
- 全国、国際での多施設共同研究の中心的役割
- 産学官共同研究の推進
胃癌、大腸癌の腹腔鏡手術に対する全国多施設共同試験を主導し、また大分県ではOITA trialを行い、大分から世界に向けたエビデンス創生に努めています。
食道癌手術の定型化
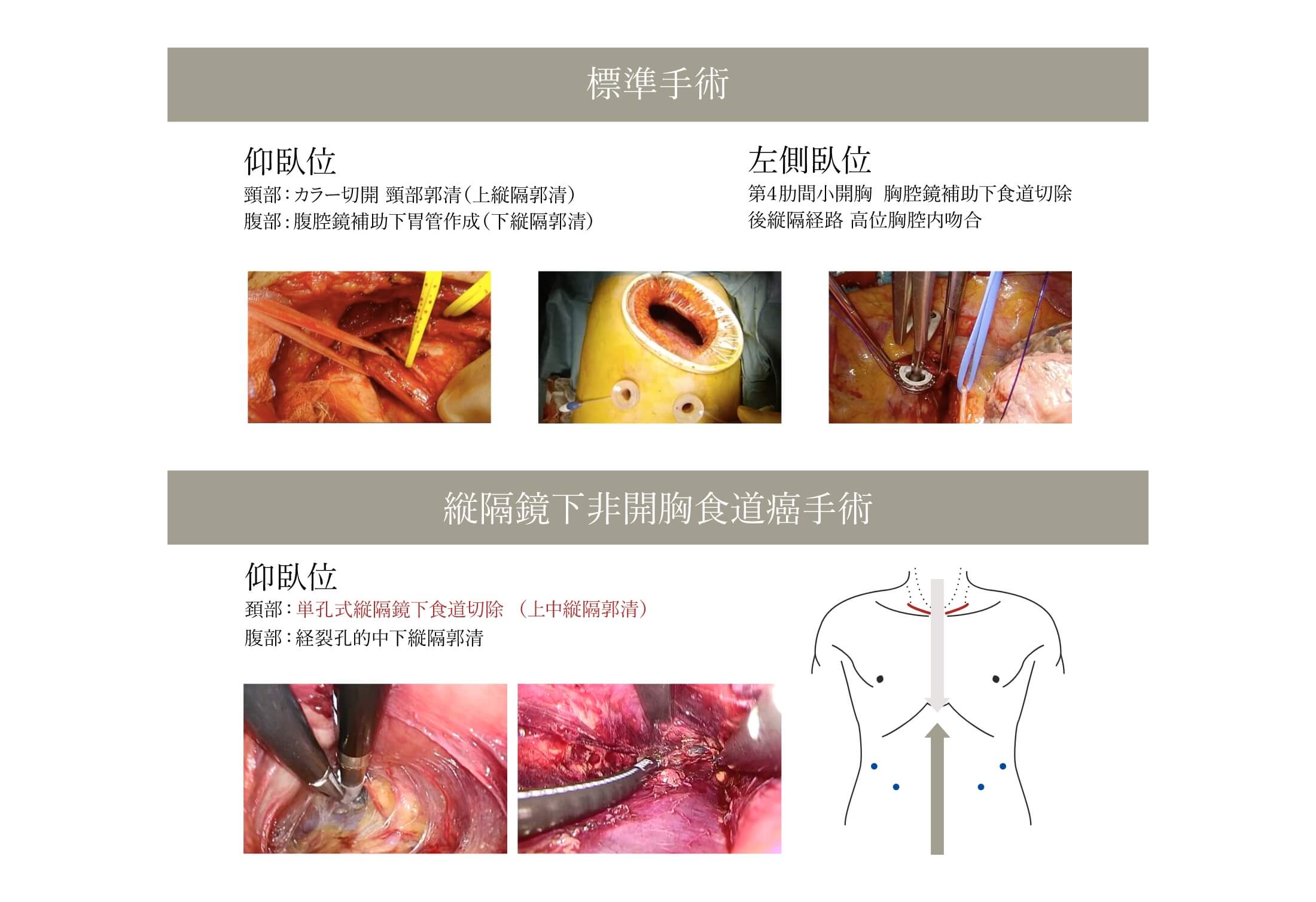
安全性・根治性・合併症予防・低侵襲性のバランスを重視し、頚部からの上中縦隔郭清と腹腔鏡による経裂孔的中下縦隔郭清を組み合わせて開胸時間を短縮する術式を標準術式としています。
開胸は腋下小切開で行い術後呼吸器合併症軽減に努めています。再建は後縦隔経路・高位胸腔内吻合を標準とし安全に施行しています。
さらに2017年より縦隔鏡下非開胸食道癌手術を導入してさらなる治療成績の向上を目指しています。
食道癌に対する集学的治療

術前から他科・メディカルスタッフ・地域中核病院と連携を取り、術後まで切れ目のない集学的治療を行なっています。
術前からリハビリ・栄養科が介入し、術前化学療法に伴う有害事象の軽減や術後合併症の予防を行い、術後も頭頚部外科との連携や早期リハビリにより、術後機能障害や能力低下の早期改善を行なっています。
新規治療として、2013年よりDCFによる術前化学療法、2018年には新たな低侵襲サルベージ治療であるPDT療法を導入し、その有効性を報告しました。
胃癌腹腔鏡手術におけるエビデンスの創出
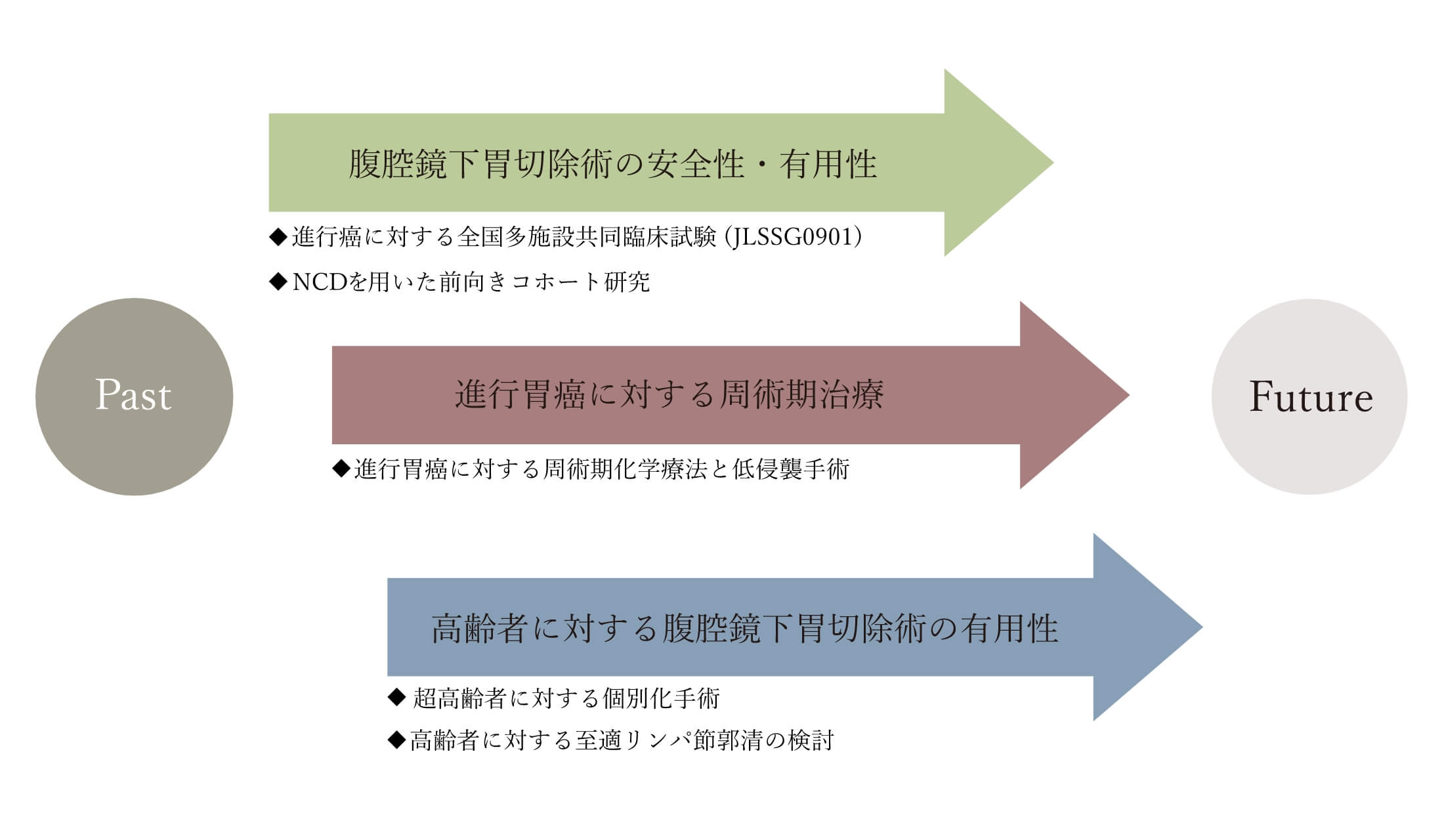
これまでに胃癌に対する腹腔鏡手術分野において、数多くのエビデンスを創出してきました。
近年では、2009年より進行胃癌に対する腹腔鏡下胃切除術の安全性を検証する全国多施設共同第Ⅲ相ランダム化比較試験の代表・事務局を担当し、短期成績における腹腔鏡下手術の安全性を報告し、長期成績についても2022年に報告予定です。さらに、周術期化学療法を施行した進行癌症例に対する腹腔鏡手術の安全性や超高齢者の特性に応じた腹腔鏡手術の有用性について研究を進めています。
個別化を目指した低侵襲手術の追求
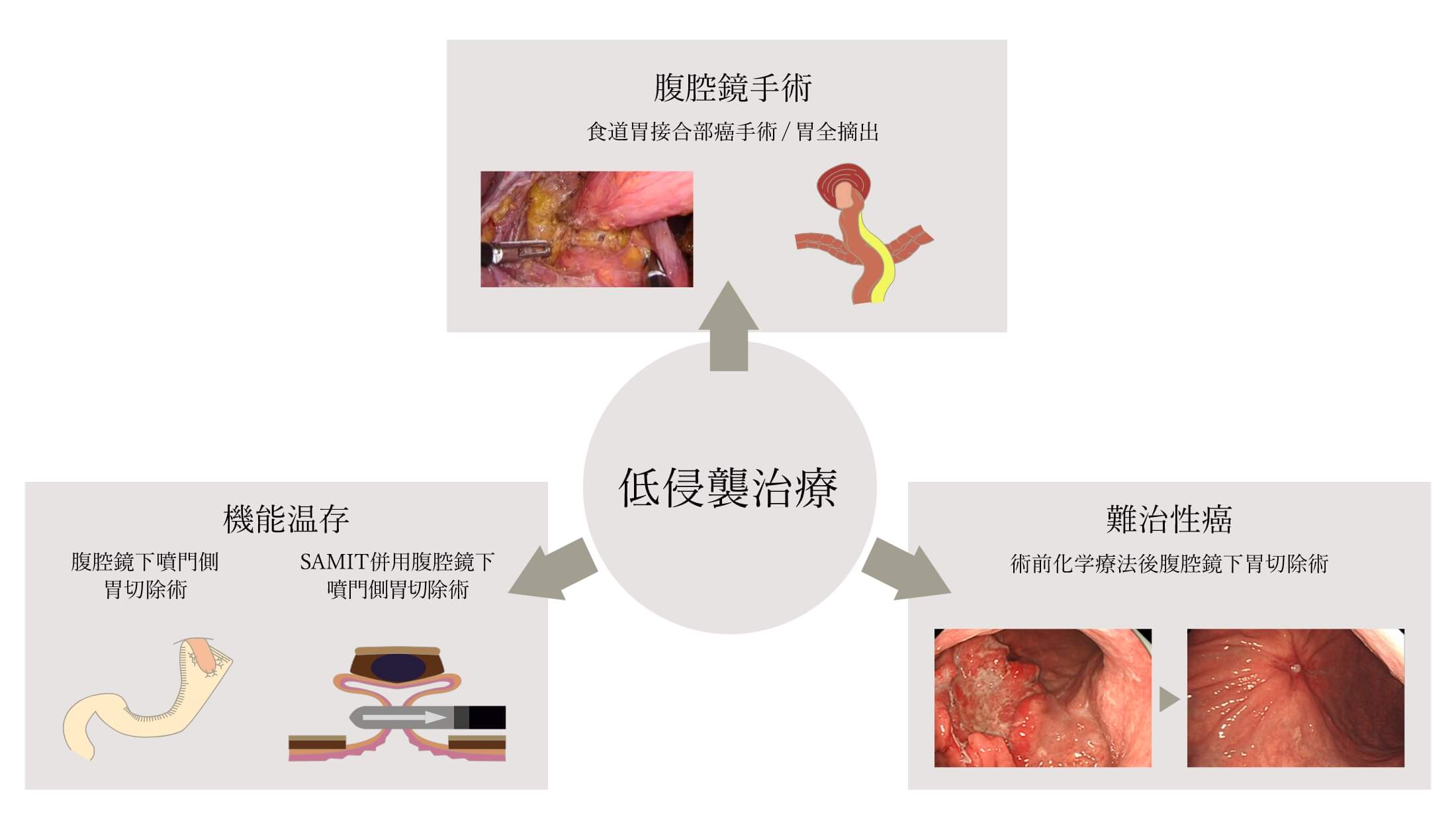
胃領域において手術治療成績の向上、また低侵襲治療の拡大のために、以下の3つの取り組みを行っています。
①上部領域癌、進行癌に対する胃全摘術、D2郭清など腹腔鏡手術の適応拡大
②腹腔鏡下噴門側胃切除術における胃内容排泄遅延を予防する細径胃管再建や、胃GISTに対する術後胃の変形を予防する漿膜筋層切開(SAMIT)を併用した腹腔鏡下胃楔状切除術などの機能温存手術
③大型3型、4型など難治性癌に対する術前化学療法後の腹腔鏡下胃切除術
新しい大腸手術手技の導入と標準化
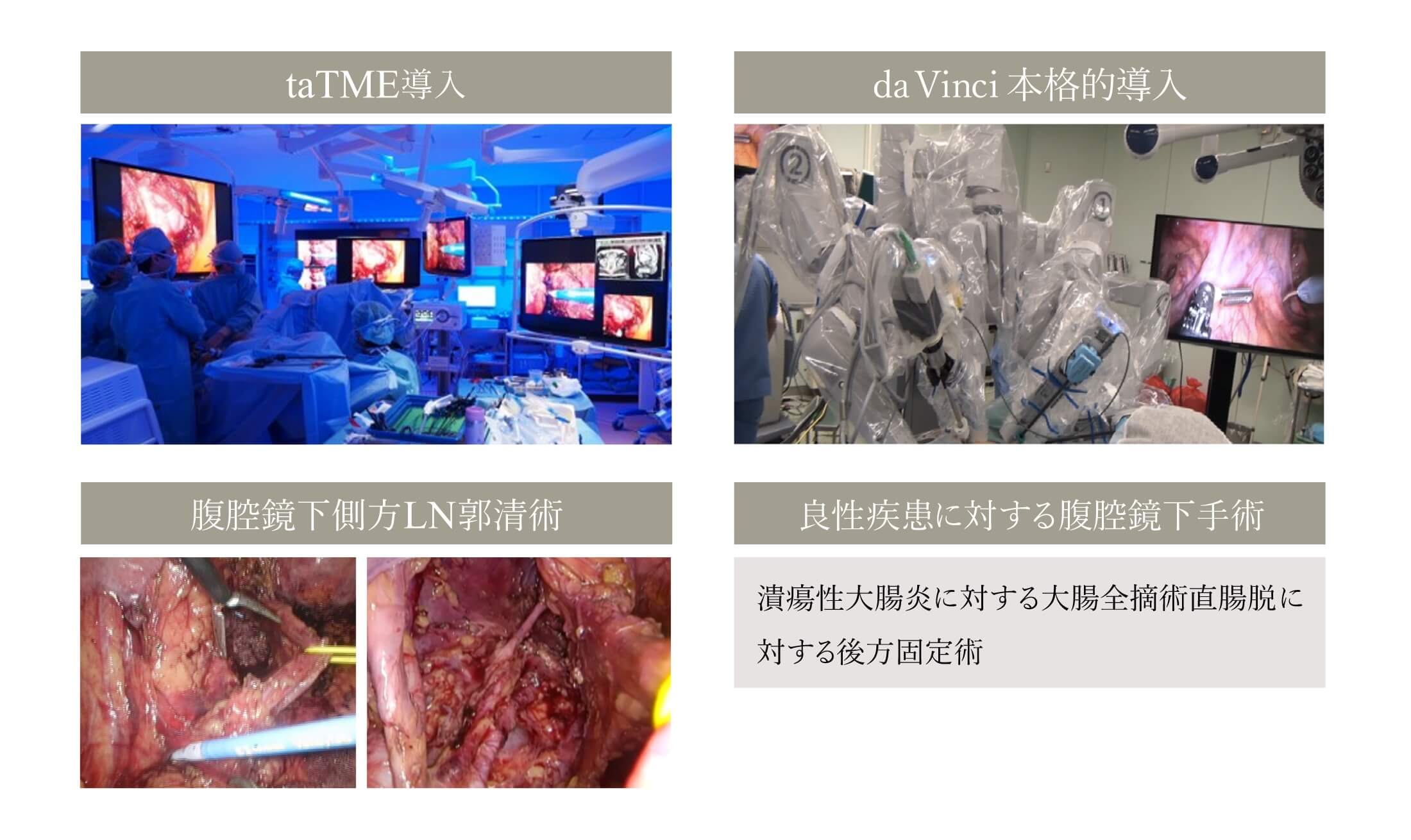
大腸領域では、新しい手技の導入および標準化を積極的に行っています。
下部直腸癌に対しては、肛門温存を確実にし、CRMの確保が可能なTaTMEやロボット手術を導入しています。経腹的だけでなく、経肛門的にも手術操作を行うTaTMEでは、新しく導入された内視鏡統合システムEndoALPHAにより、経腹操作と経会陰操作を同時に行うことが可能になりました。
さらに、転移のある側方リンパ節に対する腹腔鏡下側方郭清術も標準化を目指しています。
また、良性疾患に対しても、潰瘍性大腸炎に対する腹腔鏡下大腸全摘術や直腸脱に対する腹腔鏡下直腸後方固定術などの標準化を行っています。
大腸がんプロジェクト研究
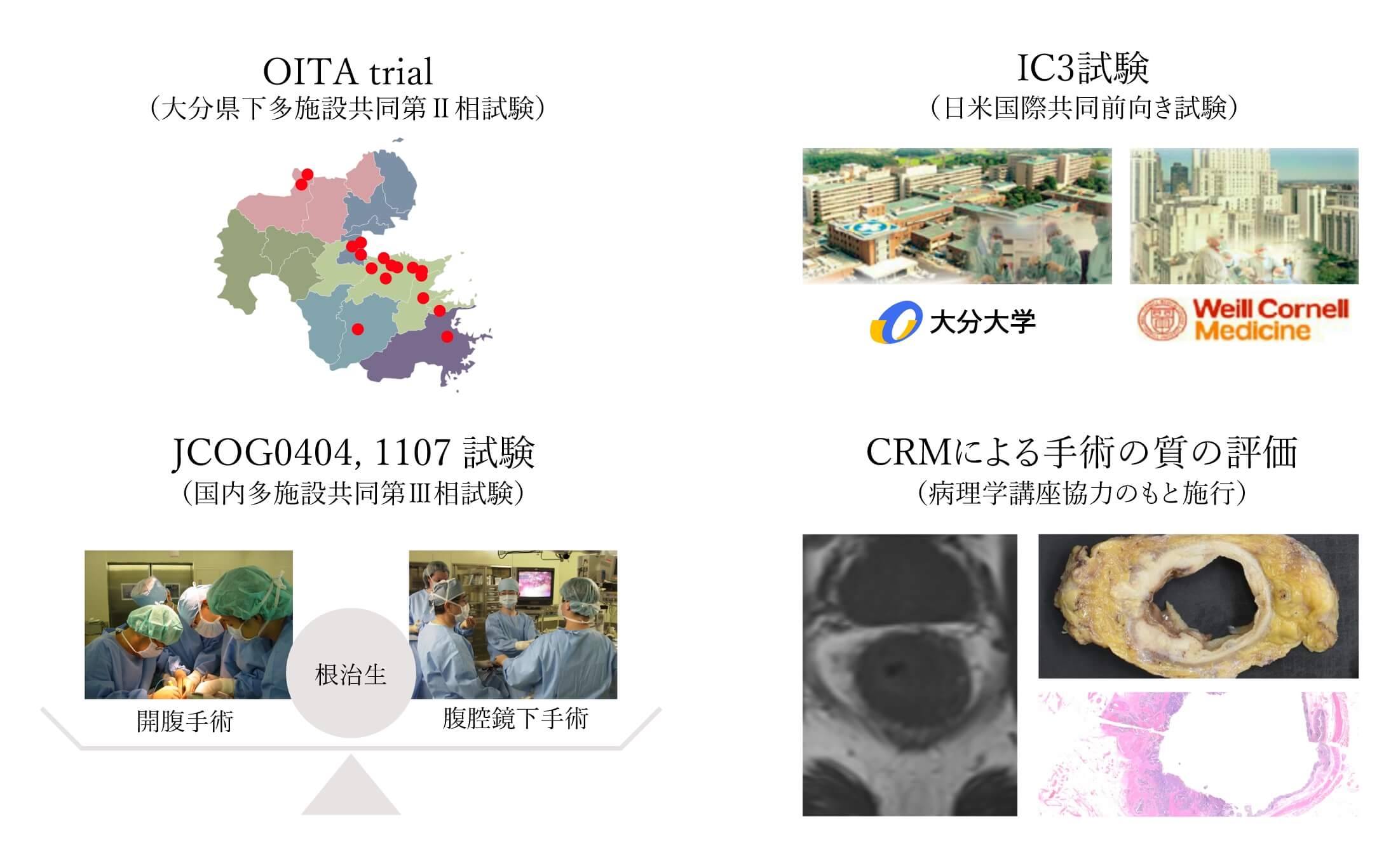
大分県、all Japan、internationalに大腸がんプロジェクト研究をすすめています。
OITA-trialは、県下の多施設共同臨床試験で、局所進行直腸癌に対して術前CRTを行う第Ⅱ相試験で、高い治療完遂率・奏効率を示しました。
JCOG大腸がんグループでは教室が代表者・事務局を務め、stageII/IIIとstageIV大腸がんに対する腹腔鏡下手術の有用性をRCTにて検証し、JCOG0404試験は主解析結果を公表し、JCOG1107試験は現在症例登録中です。
IC3試験では米国コーネル大学(Milsom教授)との国際共同前向き試験を開始し、現在症例登録中です。
また、近年直腸癌手術の質の評価としてのCRMの重要性が再認識されており、病理学講座の協力のもと画像との対比が可能な方法でCRMの評価を行なっています。
消化管外科 基礎研究
消化管外科の基礎研究テーマ三本柱
- 癌に対する新しい診断・治療法の確立
- 炎症に対する新しい治療法の開発
- 低侵襲性治療の開発
腫瘍溶解性レオウイルスを用いたがんの治療・診断用ウイルス療法の開発
がんのウイルス療法とは、がん細胞のみで増殖ができるウイルスによりがん細胞を破壊する治療法です。この「がん治療用ウイルス」の中で、当科では「レオウイルス」に着目して研究を行なっています。これまでに膵がん、胃がんや乳がんに対してもレオウイルスが有効であること報告しています(図1)。
近年では、遺伝子組換えレオウイルスの作成が可能となったことから、消化器癌の根治的治療法の確立に向けて、術中イメージング・光線力学療法に適した蛍光蛋白質を発現する遺伝子組換えレオウイルスの研究を行なっています(図2)。この蛍光発現レオウイルスにより、術中微小癌診断と殺癌細胞効果を同時に行うという診断治療一体型ナビゲーション手術の開発を目指しています。
-
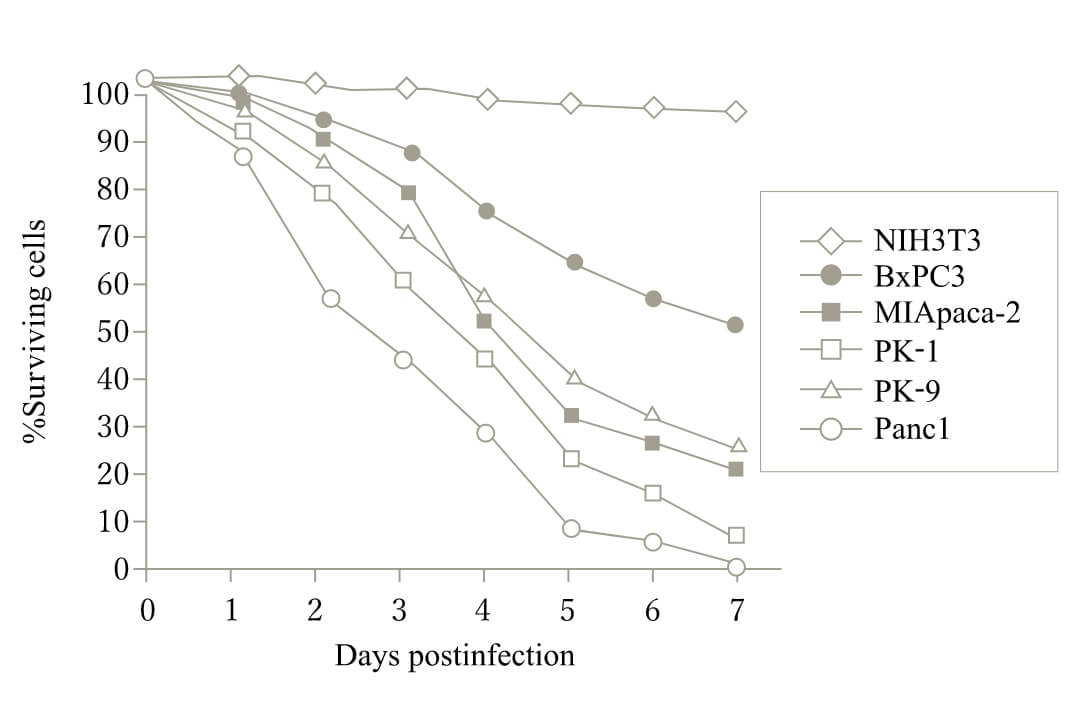
図1:レオウイルスによる抗腫瘍効果
Etoh et al. Clinical Cancer Reserch 2003 -

図2:近赤外蛍光蛋白遺伝子導入レオウイルスの蛍光発現
悪性腫瘍におけるsarcoid-like reactionの臨床病理学的意義および予後との関連
悪性腫瘍の所属リンパ節には、稀にサルコイドーシスに類似した肉芽腫形成を認める症例があることが知られており、sarcoid-like reactionと呼ばれています(図)。この組織学的変化は癌を抑制しているのではないかとの報告がありますが、その臨床病理学的意義や予後との関連には不明な点が多いのが現状です。
当科では診断病理学講座と共同し、悪性腫瘍におけるsarcoid-like reactionの意義や予後との関連を明らかにするべく研究を行っています。
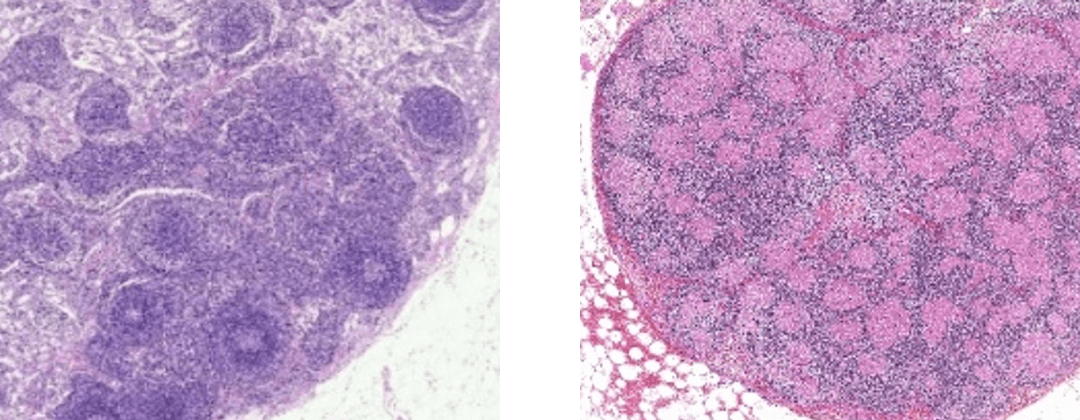 図3:悪性腫瘍の所属リンパ節 (左:正常、右:sarcoid-like reaction)
図3:悪性腫瘍の所属リンパ節 (左:正常、右:sarcoid-like reaction)
大腸癌と腸内細菌叢との関係
加齢により増加の一途を辿る大腸癌の発生機序の解明は、高齢化社会が進む中で非常に重要であると考えられます。当科では、腸内細菌叢と発癌との関連性に着目して研究を行なっています。これまで、常在性の非病原性腸内細菌叢が炎症性腸疾患(IBD)や大腸癌の発症に関与していることが示され、近年では、腸内細菌叢の変化(dysbiosis)が炎症を惹起し、発癌の原因になる可能性が示されています。しかしながら、加齢による大腸粘膜の腺管構造・大腸免疫細胞や腸内細菌叢の変化などの「腸管免疫老化」が、大腸の発癌にどのように影響しているかは明らかにされていません。現在、腸内細菌叢の中で発癌に関係していると報告のあるFusobacterium nucleatumに注目し、加齢により細菌叢内の比率が増加することで腸管免疫を変化させることで発癌に関与しているのではないかとの仮説から大腸癌の発生メカニズムの解明を進めています。
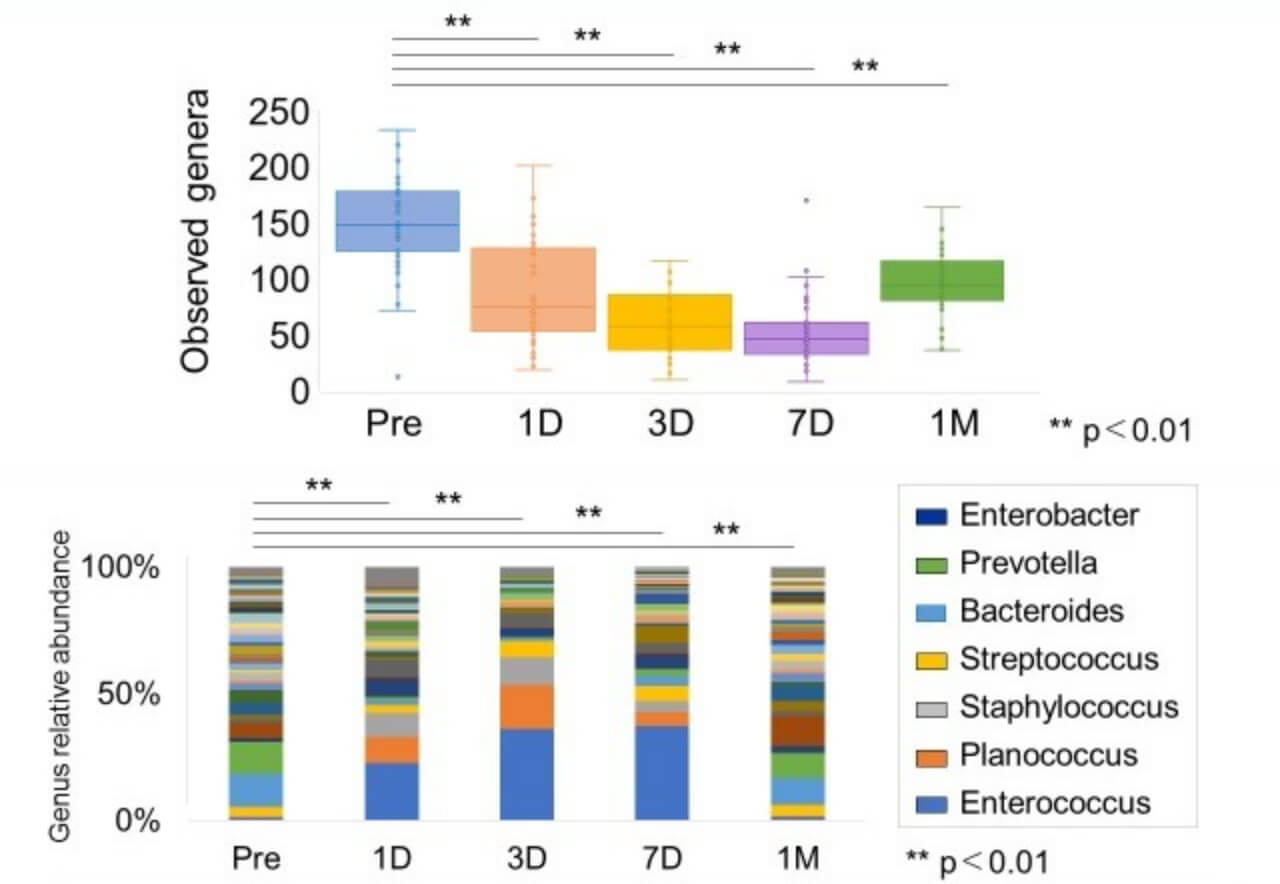 図4:周術期における腸内細菌叢の変化
図4:周術期における腸内細菌叢の変化
抗酸化剤と皮膚冷却の併用による抗癌剤脱毛予防法の開発
これまで、抗癌剤脱毛に毛包周囲の血管透過性が関与していることを明らかにしてきました1)(図5)。また、我々が開発した抗酸化剤αリポ酸には、抗癌剤脱毛の期間短縮効果があることも示してきました2)。現在、抗酸化物質αリポ酸を用いて、抗癌剤脱毛に対する皮膚冷却との併用効果を明らかにし、さらに、メカニズムとして血管透過性の制御が関与するのかを解明する研究を行っております。
蛍光標識したデキストランはcontrolに比べ、cyclophosphamide投与では血管外への漏出が見られました。
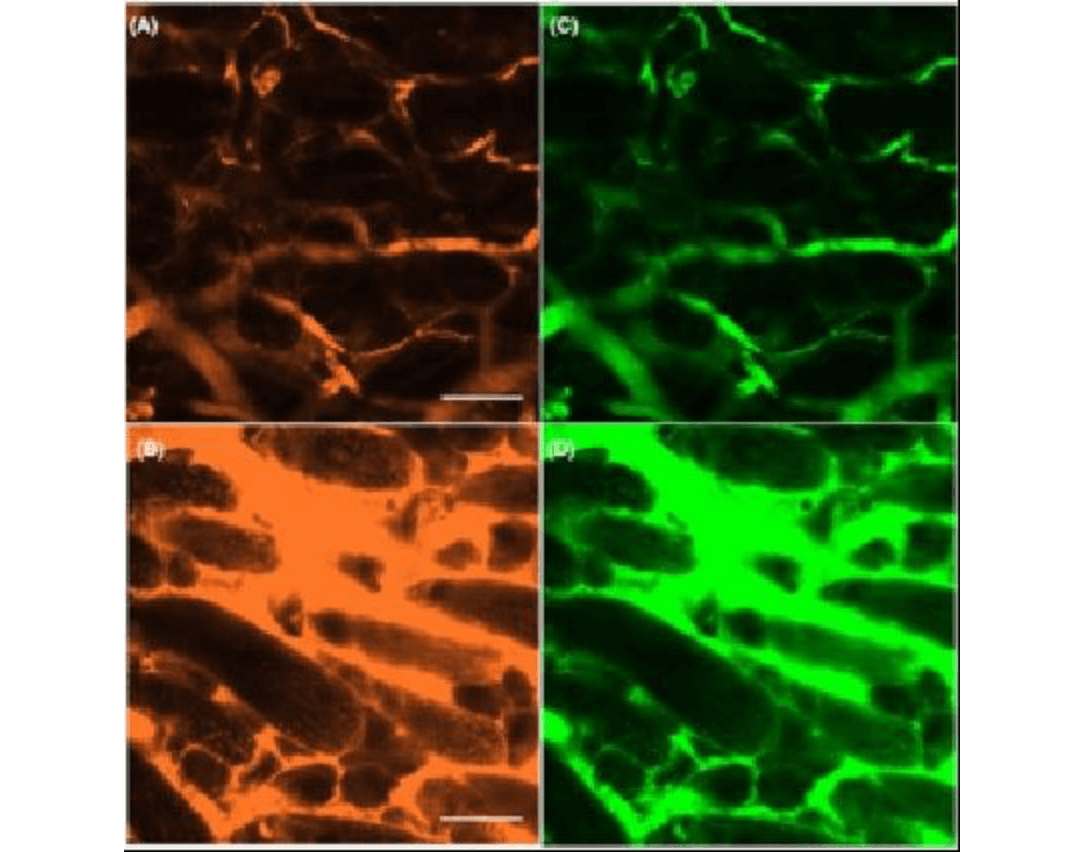 図5:蛍光デキストランによる血管透過性の評価
図5:蛍光デキストランによる血管透過性の評価
人工知能を用いた内視鏡外科手術の研究開発と外科教育への応用
胃癌に対する腹腔鏡手術は年々増加する一方、術後合併症としての膵液漏減少に対する課題は残っています。熟練の外科医はランドマークである膵臓を暗黙知し膵液漏を回避しますが、経験が浅い外科医にとっては困難な場合があり、若手外科医に対し如何に内視鏡手術を教育するかが課題となります。現在、当教室では腹腔鏡下胃切除術におけるランドマークを術中内視鏡画像に提示すAIシステムの開発を、福岡工業大学、オリンパス株式会社とともに進めています(図)。本システムは手術の安全性を高めるだけでなく、若手外科医の手術教育にも寄与することが期待されています。
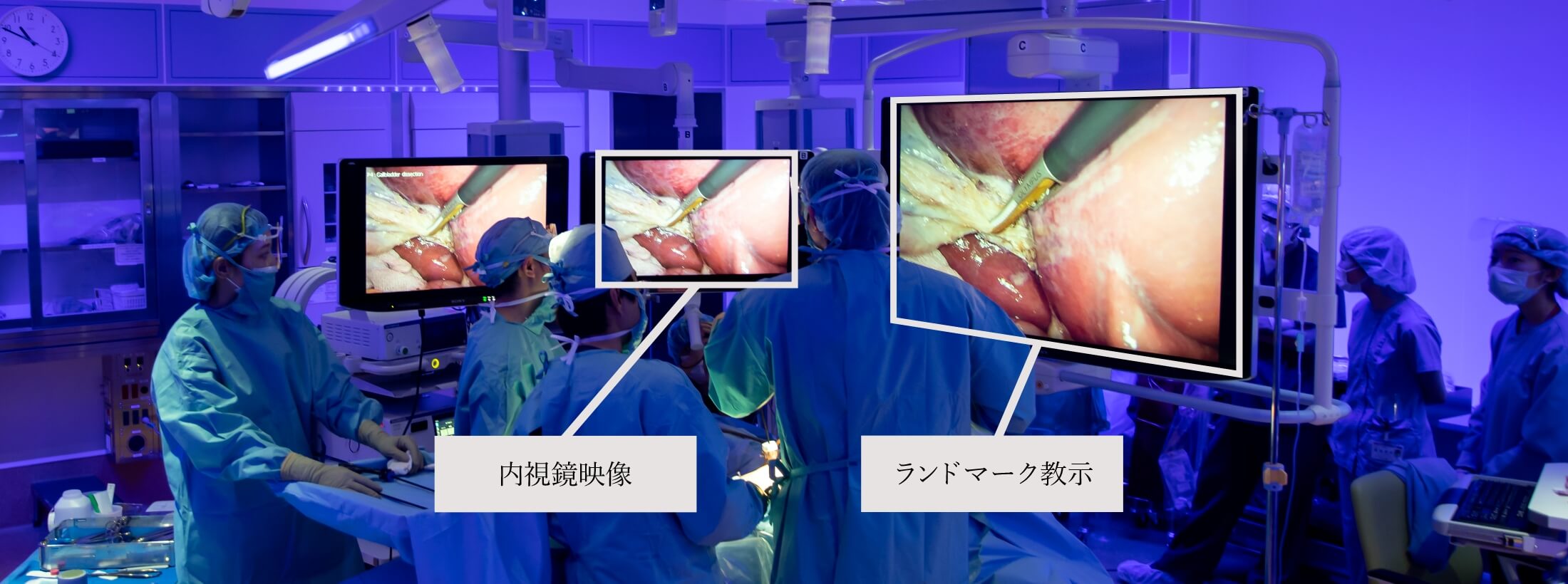 図6:腹腔鏡下胆嚢摘出術における、内視鏡画像とランドマーク教示画像
図6:腹腔鏡下胆嚢摘出術における、内視鏡画像とランドマーク教示画像内視鏡画像と並べて、リアルタイムにAIによるランドマーク教示画像が示されます。